در این فیلم آموزشی، با قانون هس و موارد استفاده آن آشنا خواهید شد.
قانون هس و محاسبه گرمای واکنش با استفاده از آن
یکی دیگر از روش های محاسبه گرمای واکنش ها، استفاده از قانون هس است. وقتی یک واکنش از نظر تجربی امکان پذیر نباشد، یا در شرایط عادی انجام آن بسیار سخت باشد یا مرحله ای از چند مرحله ی یک واکنش باشد، در این صورت گرمای واکنش به صورت مستقیم قابل محاسبه نمی باشد. در این صورت نیاز است از یک سری واکنش های دیگر برای محاسبه گرمای واکنش مورد نظر استفاده نمود. به این روش قانون هس گفته می شود.
در قانون هس، کلیه قوانین چهار عمل اصلی برقرار است. به طور نمونه یعنی اگر واکنشی را با یک واکنش دیگر جمع کنیم، آن ها نیز با جمع خواهد شد. برای حل مسئله، باید شاخص های واکنش اصلی را در نظر گرفت و محاسبات را انجام داد. در ادامه برای درک بهتر قانون هس به حل یک مثال می پردازیم.
مثال: با توجه به واکنش های زیر، آنتالپی واکنش داده شده را به دست آورید؟
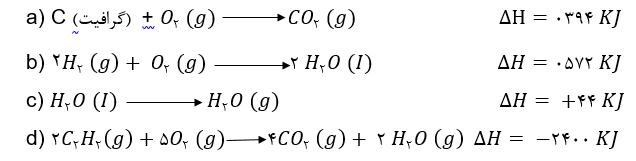
در واکنش اصلی 2 تا C داریم، بنابراین باید واکنش a را در دو ضرب کنیم. همچنین در واکنش اصلی یک دانه H2 داریم. لذا نیاز است واکنش b را در 0/5 ضرب کنیم .از C2H2 به تعداد یک عدد داریم، پس واکنش d را باید در 0.5- ضرب کنیم. در واکنش b با ضرب در 0/5 یک H2O مایع در سمت راست خواهیم داشت، پس در واکنش c نیز باید یک H2O مایع در سمت چپ داشته باشیم. بنابراین واکنش c در عددی ضرب نخواهد شد. پس برای محاسبه کلΔH ، رابطه زیر را خواهیم داشت.
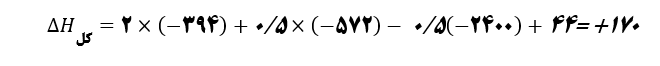
یکی دیگر از روش ها به منظور محاسبه گرمای واکنش، قانون هس می باشد.
به منظور یادگیری بیشتر قانون هس، نکات و نمونه سوالات تستی آن می توانید ویدئو آموزشی را مشاهده کنید.
سوالات متداول
به روشی که در آن از واکنش های دیگر برای محاسبه گرمای واکنش استفاده می شود، قانون هس گفته می شود.
بله در قانون هس، کلیه قوانین چهار عمل اصلی برقرار می باشد. یعنی اگر واکنشی را با یک واکنش دیگر جمع کنیم، ΔH آن ها نیز با یکدیگر جمع خواهد شد. اگر واکنش را در یک واکنش دیگر ضرب کنیم، ΔH آن ها نیز در یکدیگر ضرب خواهد شد و اگر این دو واکنش را بر یکدیگر تقسیم کنیم، ΔH آن ها نیز بر همدیگر تقسیم خواهد شد. اگر واکنش را برعکس کنیم Δ نیز قرینه خواهد شد.
یکی دیگر از روش هایی که به منظور محاسبه گرمای واکنش ها کاربرد دارد، قانون هس می باشد. قانون هس در مواردی کاربرد دارد که امکان انجام یک واکنش از نظر تجربی وجود نداشته باشد، در شرایط عادی انجام واکنش مورد نظر بسیار سخت باشد یا مرحله ای از چند مرحله ی یک واکنش باشد. در این شرایط، گرمای واکنش را به صورت مستقیم نمی توان حساب نمود و باید از واکنش های دیگر برای به دست آوردن گرمای واکنش استفاده نمود. در واقع باید از قانون هس در این مواقع استفاده کرد.





