در این فیلم آموزشی، با مباحث لازم جهت انجام محاسبات در شیمی مانند واحد کربنی، مول، جرم مولی و جرم اتمی میانگین آشنا خواهید شد. با یادگیری موارد ذکر شده، قادر به حل تست های کنکور سراسری خواهید بود.
واحد کربنی
اتمها بسیار ریزند به طوری كه نمیتوان آنها را به طور مستقیم مشاهده و جرم آنها را اندازهگیری کرد؛ به همین دلیل دانشمندان مقیاس جرم نسبی را برای تعیین جرم اتمها به كار میبرند. واحد کربنی که به آن amu میگویند، مقداری برابر با 1/12 جرم اتم کربن 12 می باشد.
با تعریف amu، شیمیدانها موفق شدند جرم اتمی دیگر عنصرها و همچنین جرم ذرههای زیراتمی را اندازهگیری كنند. در این مقیاس جرم پروتون و نوترون در حدود amu1 بوده در حالیکه جرم الکترون 1/2000 amu میباشد.
مول و جرم مولی
مول: یک واحد شمارشی است. به تعداد 1023×6/022 ذره از هر ماده، یک مول گفته می شود. به عنوان مثال 1023×6/022 ذره از هر اتم، یک مول از آن اتم محسوب می شود.
جرم مولی: برابر با جرم یک مول ماده میباشد. یکای جرم مولی برابر با g × mol-1 است.
در شیمی، جرم مولی برابر با جرم یک مول ماده می باشد.
جرم اتمی میانگین
جرم اتمی میانگین: برای تعیین جرم اتمی میانگین، باید فراوانی ایزوتوپ ها را داشته باشیم. برای محاسبه جرم اتمی میانگین، فراوانی هر ایزوتوپ (یا درصد فروانی) را در عدد جرمی آن ضرب می کنیم، سپس جمع این اعداد را بر مجموع فروانی ها (درصد فروانی ها) تقسیم کنیم.
به طور نمونه، کلر از دو ایزوتوپ با عدد جرمی 35 و 37 تشکیل شده است. فروانی ایزوتوپ با عدد جرمی 35 برابر سه و فروانی ایزوتوپ با عدد جرمی 37 برابر یک می باشد.
جرم اتمی میانگین کلر به صورت زیر محاسبه خواهد شد:
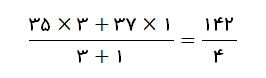
اگر در مثال بالا، به جای فراوانی، درصد فراوانی ایزوتوپ ها داده شده بود، یعنی، درصد فروانی ایزوتوپ با عدد جرمی 35 برابر با 75% و درصد فروانی ایزوتوپ با عدد جرمی 37 برابر با 25% بود. در این حالت جرم اتمی میانگین به شکل زیر به دست خواهد آمد:
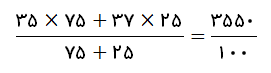
به منظور تعیین جرم اتمی میانگین، نیاز است فراوانی ایزوتوپ ها را داشته باشیم.
مثال
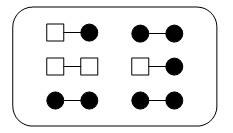
تست: با توجه به شکل مقابل، جرم مولی میانگین گاز کلر کدام است؟
1) 66/70
2) 33/71
3) 71
4) 5/71
پاسخ: گزینه 2 پاسخ صحیح می باشد.
به منظور یادگیری بیشتر مول، جرم مولی و جرم اتمی میانگین می توانید ویدئو آموزشی را مشاهده کنید.
سوالات متداول
جرم مولی، برابر با جرم یک مول از هر ماده ای می باشد.
واحد کربنی به 1/12 جرم اتم کربن 12 گفته می شود.
به منظور تعیین جرم اتمی میانگین، نیاز است فراوانی ایزوتوپ ها را داشته باشیم. برای محاسبه جرم اتمی میانگین، فراوانی هر ایزوتوپ (یا درصد فروانی) را در عدد جرمی آن ضرب خواهیم کرد، سپس جمع این اعداد را بر مجموع فروانی ها (درصد فروانی ها) تقسیم می کنیم.